Forskere har identifisert tette mikroskopiske strukturer i blodet hos Long COVID-pasienter: mikroklumper som er sammenvevd med nøytrofile ekstracellulære feller (NETs). Funnene, publisert i Journal of Medical Virology, peker mot en mulig forklaring på vedvarende symptomer og antyder nye behandlingsspor. Dette er første gang den nære strukturelle koblingen mellom mikroklumper og NETs er dokumentert.
Kjernen i funnet
- Hos Long COVID-pasienter er mikroklumper tett viklet sammen med NETs.
- Strukturene forekommer langt oftere enn hos friske kontrollpersoner.
- De er større, tettere og betydelig vanskeligere for kroppen å bryte ned.
- Dette kan blokkere de minste blodårene og redusere oksygentilførselen til vev.
Nøytrofile ekstracellulære feller (NETs) er klebrige proteinnett som immunceller danner for å fange og bekjempe infeksjoner.
Hvem står bak, og hvor er det publisert?
Studien er et samarbeid mellom professor Resia Pretorius ved Stellenbosch University (Sør-Afrika) og doktor Alain Thierry ved Montpellier Cancer Institute (Frankrike). Resultatene er publisert i Journal of Medical Virology.
Slik ble det påvist
Forskerne brukte bildestrømningscytometri og fluorescensmikroskopi for å gjøre en kvantitativ og strukturell analyse av blodprøver fra Long COVID-pasienter sammenlignet med friske kontrollpersoner.
- Biomarkører knyttet til både mikroklumper og NETs var markant økt hos pasientene.
- Mikroklumpene var flere i antall og vesentlig større i pasientprøvene.
Hvorfor kan dette forklare symptomene?
Mange med Long COVID rapporterer utmattelse, pusteproblemer, hjernetåke og redusert fysisk kapasitet. De nye funnene gir en mulig biologisk forklaring: blokkerte mikrokar kan redusere oksygentilførselen til vev og påvirke kroppens vitale funksjoner.
Strukturene var større, tettere og vanskeligere å bryte ned hos Long COVID-pasienter enn hos friske.
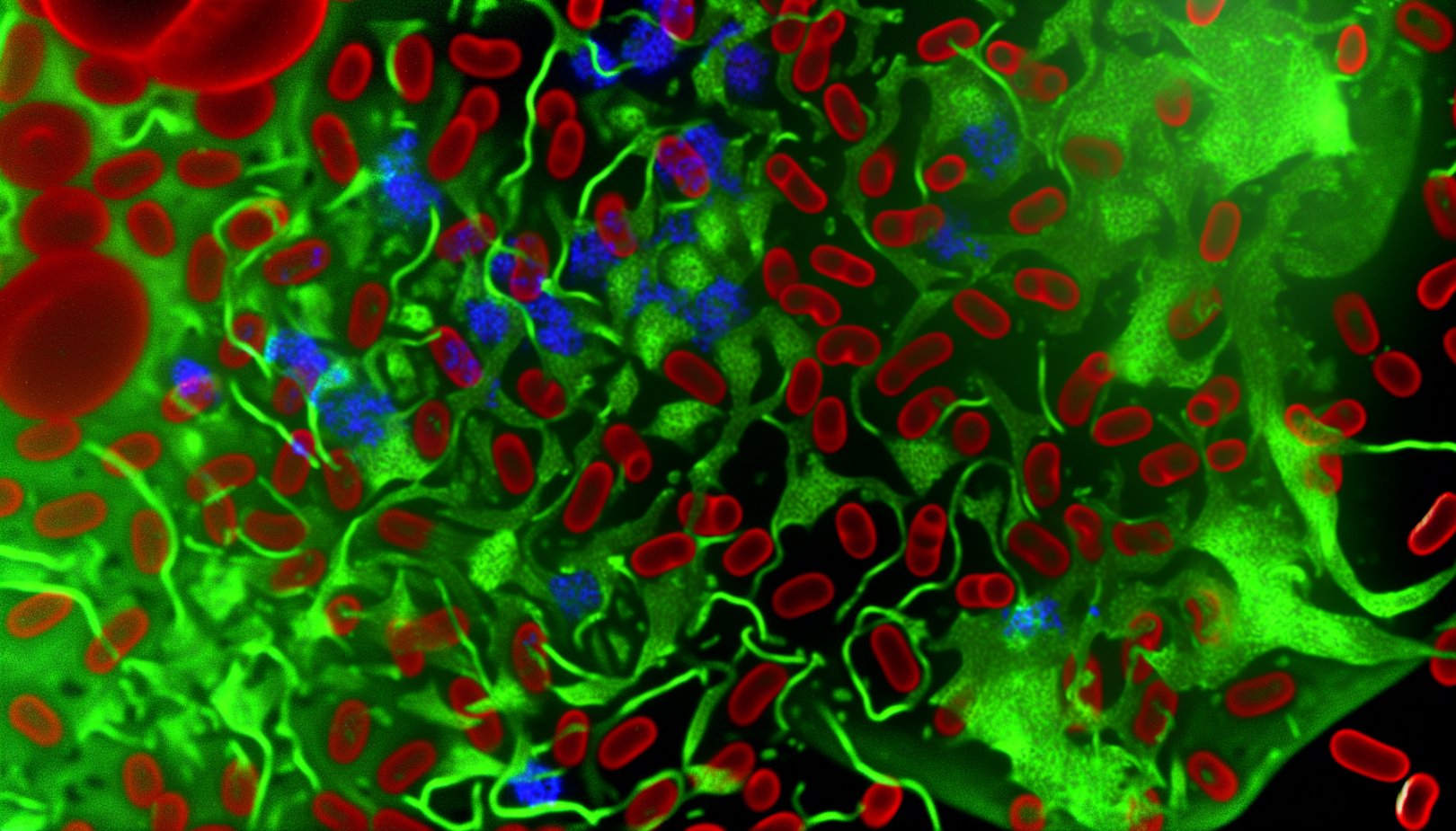
Hva viser bildene?
Under mikroskopet fremstår strukturene som tette klumper der grønne områder viser unormale, klebrige proteinnett, mens røde og blå områder stammer fra immuncellemateriale fanget inne i mikroklumpen. Sammen danner de kompakte formasjoner som potensielt kan blokkere små blodårer.
Vanskelig å bryte ned
Forskerne peker på at interaksjonen mellom mikroklumper og NETs kan gjøre klumpene mer motstandsdyktige mot fibrinolyse – kroppens naturlige prosess for å løse opp blodpropper. Dette kan fremme vedvarende sirkulasjon av klumpene og bidra til kroniske mikrovaskulære komplikasjoner.
Kroppens mekanisme for å bryte ned blodpropper. Økt motstand mot fibrinolyse kan forlenge levetiden til mikroklumper i blodbanen.
Hva betyr dette for behandling?
Oppdagelsen kan få betydning for fremtidig behandling. Funnene peker mot mulige terapeutiske tilnærminger som retter seg mot å redusere skadelig koagulering og betennelse hos Long COVID-pasienter. Studien bidrar også til økt forståelse av hvordan mikroklumper oppstår og vedvarer i sirkulasjonssystemet.
Dette er ikke første gang mikroklumper er koblet til Long COVID, men det er første gang den nære strukturelle koblingen til immunforsvarets klebrige nett er dokumentert – en viktig puslespillbrikke i arbeidet med å forstå og behandle de langvarige effektene av COVID-19.
Kilder: ScienceDaily, EurekAlert, Medical Xpress, Journal of Medical Virology
Kort oppsummert: Forskere har for første gang dokumentert en tett sammenveving av mikroklumper og NETs i blodet til Long COVID-pasienter. Strukturene er hyppigere, større og mer motstandsdyktige enn hos friske – og de kan hemme oksygentilførselen ved å tette de minste blodårene. Dette åpner for nye mål i behandling og videre forskning.










Kommentarer
0 kommentarer
Vi godtar kun kommentarer fra registrerte brukere. Dette gjør vi for å opprettholde en trygg og respektfull debatt, samt for å unngå spam og misbruk. Registrering er gratis og tar bare noen sekunder.
Du må være innlogget for å kommentere. Logg inn eller registrer deg for å delta i diskusjonen.